Results and discussion
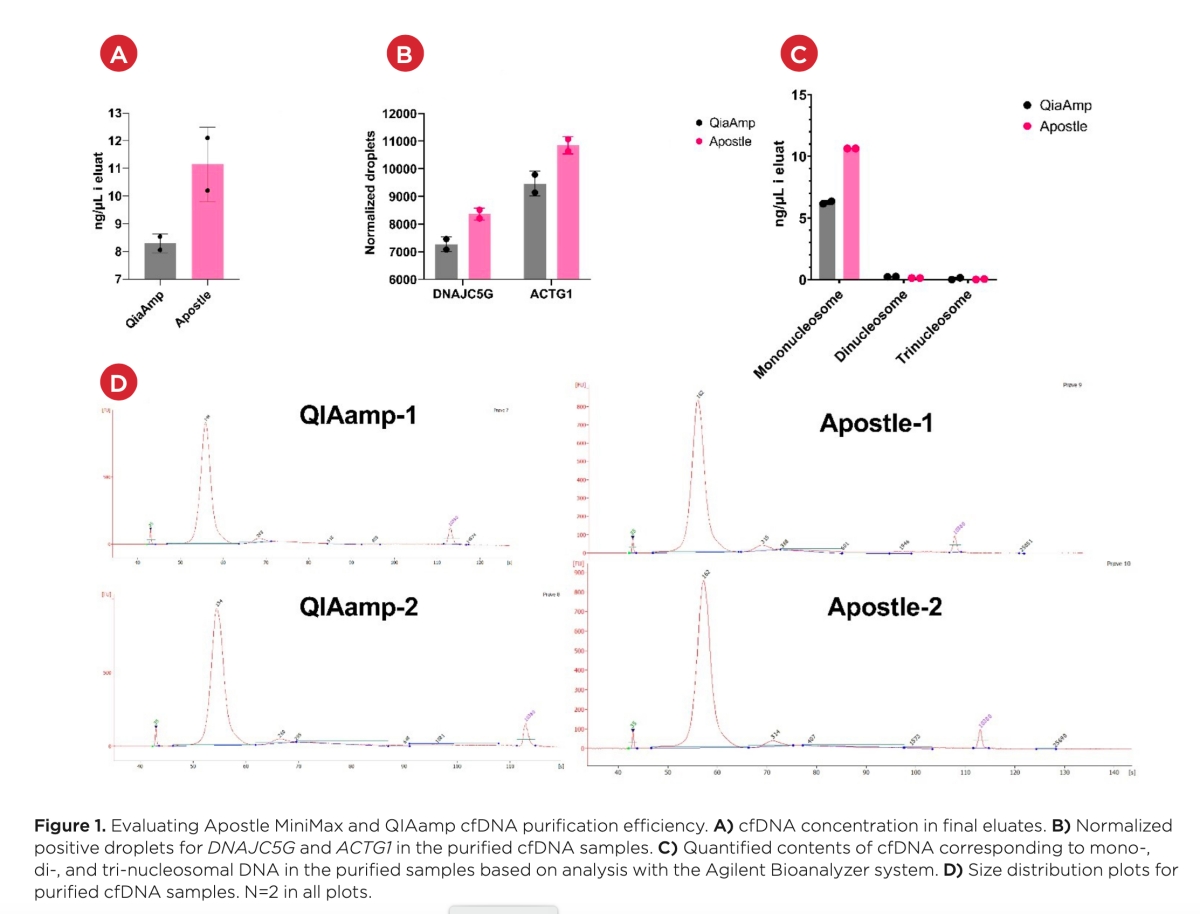
Mean cfDNA concentrations in the eluates were determined to be 8.30 ng/μL for samples extracted with the QIAamp kit and 11.15 ng/μL for samples extracted with the Apostle kit when measured with the Qubit assay (Figure 1A). This illustrates a 34.3% higher yield when using the Apostle kit as compared to the QIAamp kit.
When evaluating the contents of specific genes in the eluate, the Apostle purification displayed a higher yield than QIAamp (Figure 1B). 8358 DNAJC5G positive droplets were detected in the Apostle samples compared to 7269 droplets in the QIAamp samples. Similarly, 10849 ACTG1 droplets were detected in the Apostle-extracted samples versus 9463 droplets detected in the QIAamp-extracted samples. This data demonstrates an average of 14.8% higher yield using the Apostle kit.
Finally, when evaluating cfDNA fragments via the Agilent bioanalyzer instrument, the Apostle kit demonstrated the highest yield (Figure 1C and D). Mononucleosomal cfDNA concentration in the eluate of Apostle samples was estimated to be 10.64 ng/μL versus 6.26 ng/μL in the eluate of QIAamp samples. The dinucleosomal cfDNA concentration was low for both kits, with 0.13 ng/μL recorded for Apostle samples and 0.24 ng/μL for QIAamp samples. This indicates a slightly better purification of dinucleosomal cfDNA using QIAamp; however, this could also be an artifact given the low concentrations. The Apostle mononucleosomal cfDNA yield was 70.0% higher than the yield for the QIAamp samples.
Publication: Comparative analysis of cell-free DNA extraction efficiency from plasma. Beckman Coulter Life Sciences. Indianapolis, IN. Technical Note 2022.